|
|

|
|
|

Relativna
atomska masa elementa |
|
|
|
|
Broj
na vrhu kućice označava relativnu atomsku masu elementa točnu
do četvrte decimale.
( ) - označavaju masu najstabilnijeg izotopa.
*Razlika relativne atomske mase i rednog broja elementa je broj
protona u jezgri. |
|
|
|
|
|

Kemijski
simbol elementa |
|
|
|
|
U
sredini kućice se nalazi od IUPAC-a i međunarodno priznat
kemijski simbol elementa.
Ako je simbol sive boje to znači da još nije sintetiziran.
*Svi transuranski elementi (ili transaktinidni) se mogu dobiti
samo sintetski, tj. još uvijek nisu otkriveni u nekoj od ruda
(npr. uranovom smolincu). Razlog tomu je izuzetno kratak
poluraspad, tako da takav element ni u kom slučaju ne može
postojati neko duže vrijeme u slobodnom stanju, ili u spojevima.
Najčešće se dobivaju u vrlo malim količinama, pa čak i svega
nekoliko atoma (Uuo). |
|
|
|
|
|
Redni
(ili atomski) broj elementa |
|
|
|
|
Broj
na dnu predstavlja redni broj elementa i broj protona koje sadrži
njegova jezgra. |
|
|
|
|
|

Kemijska
skupina elementa |
|
|
|
|
|
|
|
|

Agregatno
stanje elementa |
|
|
|
|
U
donjem lijevom kutu je kućica koja svojom bojom pokazuje
agregatno stanje elementa uz normalan tlak - (101325 Pa) i
temperaturu - 20°C (293,15 K). Agregatna stanja:
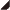 |
-
Kruto |
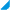 |
-
Tekuće |
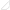 |
-
Plinovito |
*Za
sve elemente agregatno stanje je sigurno, ili se sa velikom
sigurnošću pretpostavlja, no za novootkrivene Uub (tekući?) i
Uuo (plinoviti?) se samo nagađa jer su dobivene količine smiješno
male (samo nekoliko atoma), no radi periodičnosti PSE mogli bi
imati svojstva kao i elementi iznad. Uub\Hg, Uuo\Rn. Ono što
stvara dvojbe je njihova ogromna relativna atomska masa, tako da
je ipak malo vjerojatno da bi tako teški elementi mogli biti u
nekom drugom stanju osim krutoga. No ipak, ako pretpostavimo da
su međumolekulske sile među njima zanemarivo male onda bi takva
agregatna stanja bez obzira na masu bila moguća. |
|
|
|
|
|

Kemijska
grupa elementa |
|
|
|
|
|
|
|
|

Radioaktivan
kemijski element |
|
|
|
|
Simbol
opasnosti od ionizirajućeg zračenja stoji uz svaki element
kojemu je broj stabilnih atoma manji od broja onih koji podliježu
spontanom raspadu.
*Svi umjetno dobiveni elementi su radioaktivni. |
|
|
|
|
|

Sintetski
dobiven element |
|
|
|
|
Bijela
pruga (na slici je crna radi uočljivosti) stoji za sintetski
dobivene elemente. Kao što je navedeno iznad - svi sintetski
elementi su radioaktivni. Dobivaju se u laboratorijima ili u
industriji (najčešće u nuklearnim elektranama). |
|
|
|
|
|
Kemijske
grupe; broj elektrona u zadnjoj ljusci |
|
|
|
|
Iznad
periodnog sustava se nalaze brojevi prema kojima se može zaključiti
broj elektrona u zadnjoj atomskoj ljusci. Ovdje su navedena dva
sustava prikazivanja; onaj s rimskim brojem i slovom pokraj je
IUPAC-ov standard iz 1970, u drugom slučaju su se koristile
arapske brojke i to od 0 do 18. To je novi IUPAC-ov standard iz
1989. |
|
|
|
|
|
|
|
|
Sa
lijeve strane periodnog sustava se nalaze brojevi od jedan do šest,
koji se nazivaju periodama. Vrijednost svake periode označava
broj elektronskih ljuski koje elementi na desno imaju (vodoravno). |
|
|
 |
|